 Cr2(so4)3=k2cr k2cr2o7. 2cr3+3s=cr2s3. K2so3 k2s. Метод ионно электронного баланса kmno4 + k2s + h2so4. Cr203+h2so4.
Cr2(so4)3=k2cr k2cr2o7. 2cr3+3s=cr2s3. K2so3 k2s. Метод ионно электронного баланса kmno4 + k2s + h2so4. Cr203+h2so4.
|
 Kmno4 степень окисления. K2so3 k2s. So2 so3. Mn в кислой среде. S+h2so4 конц.
Kmno4 степень окисления. K2so3 k2s. So2 so3. Mn в кислой среде. S+h2so4 конц.
|
 K2so3 k2s. K2so3 k2s. K2so3 k2s. H2s04+k20. Cr cro3 h2cr2o7 k2cro7.
K2so3 k2s. K2so3 k2s. K2so3 k2s. H2s04+k20. Cr cro3 h2cr2o7 k2cro7.
|
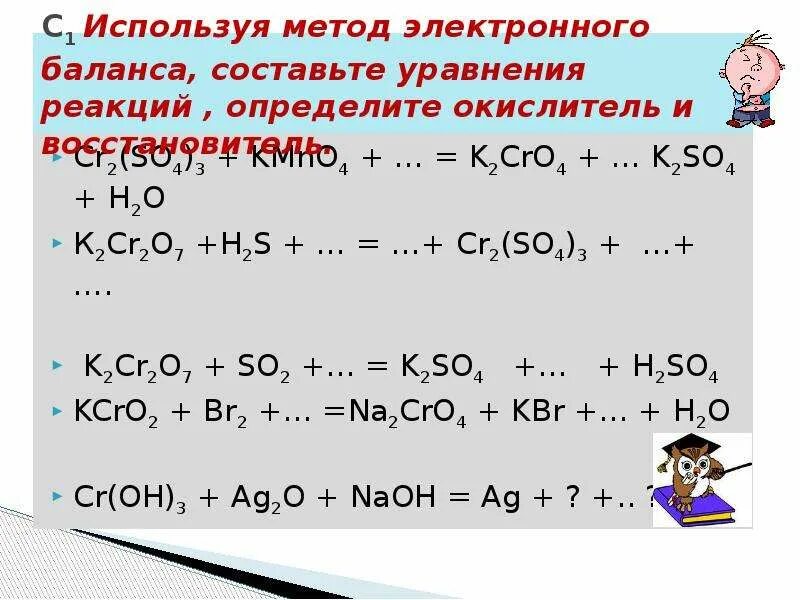 K+h2so4 + h2 электронные баланс. K2s окислитель или восстановитель. K2so3 k2s. 3s 6koh 2k2s k2so3 3h2o тип овр. Реакции h2so3 + основание.
K+h2so4 + h2 электронные баланс. K2s окислитель или восстановитель. K2so3 k2s. 3s 6koh 2k2s k2so3 3h2o тип овр. Реакции h2so3 + основание.
|
 K2cr2o7 восстановитель. So2 2- окислитель или восстановитель. K2so4 k2s. K2so3 k2s. K2so3 k2s.
K2cr2o7 восстановитель. So2 2- окислитель или восстановитель. K2so4 k2s. K2so3 k2s. K2so3 k2s.
|
 S+koh=k2s+k2s2o3. K2cr2o7. Mn в нейтральной среде. 2cr 3h2so4 cr2 so4 3. K2so3 k2s.
S+koh=k2s+k2s2o3. K2cr2o7. Mn в нейтральной среде. 2cr 3h2so4 cr2 so4 3. K2so3 k2s.
|
 K2o+mg+h2so4. Mn+2 щелочная среда. K2so4 s. Kmno4+ h2o2. Mn04 mno2.
K2o+mg+h2so4. Mn+2 щелочная среда. K2so4 s. Kmno4+ h2o2. Mn04 mno2.
|
 K2so3 k2s. H2so3 окислитель и восстановитель. Fe+s=fe2s2. K2so3 k2s. K2so3 k2s.
K2so3 k2s. H2so3 окислитель и восстановитель. Fe+s=fe2s2. K2so3 k2s. K2so3 k2s.
|
 Mno2 плюс hcl. Mno4- mn+2 - в кислой среде. Kmno4 k2so3 h2so4 овр. Cr(oh)3 h2s. Cr3+ cr2o2–.
Mno2 плюс hcl. Mno4- mn+2 - в кислой среде. Kmno4 k2so3 h2so4 овр. Cr(oh)3 h2s. Cr3+ cr2o2–.
|
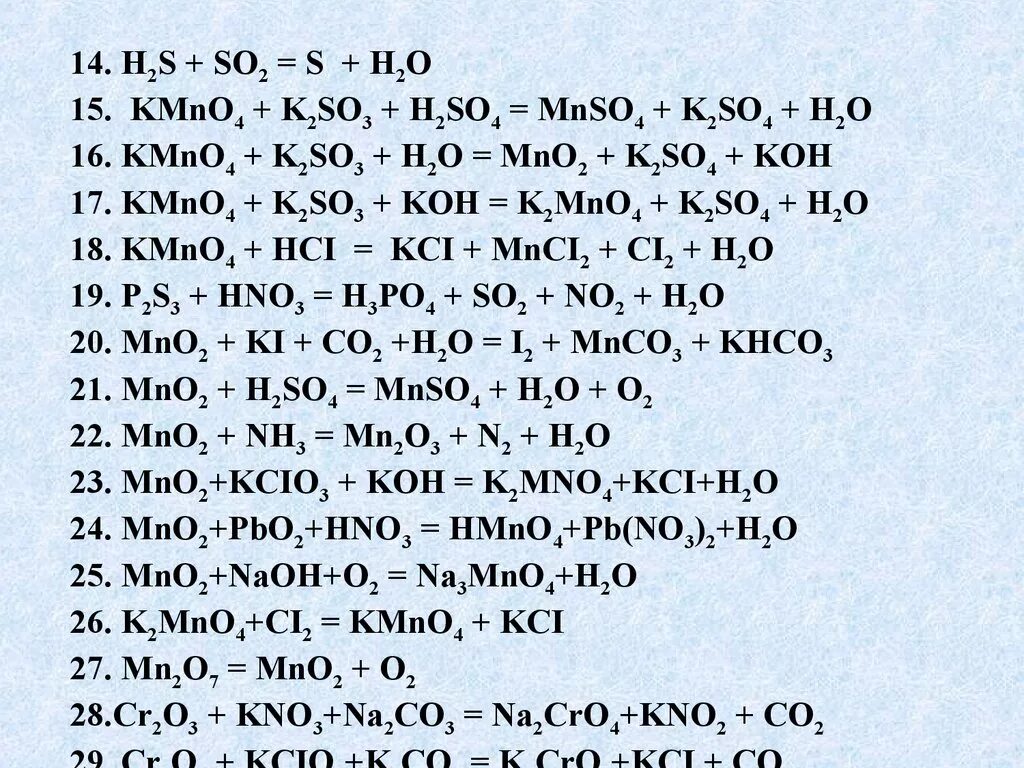 Определить степень окисления kmno4. K2cr2o7 s cr2o3 k2so4 овр. Fe2(so4)3 + k2s. H2o2 овр полуреакции. Cr o h2 cr o4.
Определить степень окисления kmno4. K2cr2o7 s cr2o3 k2so4 овр. Fe2(so4)3 + k2s. H2o2 овр полуреакции. Cr o h2 cr o4.
|
 Mnso4+k2so4+h2o. K2so3 k2s. K2cr2o7 окислитель. H2+s= h2sокислительно восстановительная. Cr2so4 цвет.
Mnso4+k2so4+h2o. K2so3 k2s. K2cr2o7 окислитель. H2+s= h2sокислительно восстановительная. Cr2so4 цвет.
|
 Cu kmno4 h2o. Kmno4 h2so4 h2o. K2s kmno4 h2o mno2 s koh окислительно восстановительная реакция. Степень окисления среды. Fe2s +02.
Cu kmno4 h2o. Kmno4 h2so4 h2o. K2s kmno4 h2o mno2 s koh окислительно восстановительная реакция. Степень окисления среды. Fe2s +02.
|
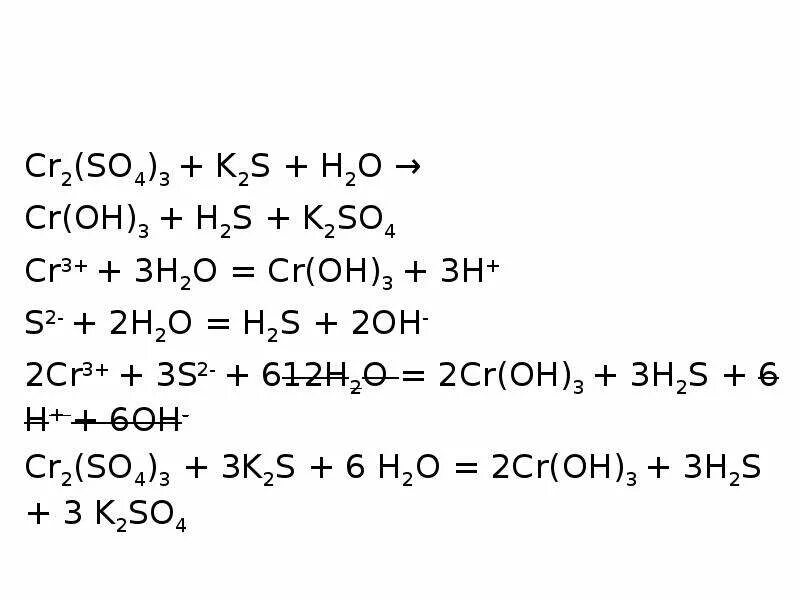 K2so3 k2s. K2so3 k2s. K2cr2o7 s. Kmno4 k2so3 h2o овр. Fe2s.
K2so3 k2s. K2so3 k2s. K2cr2o7 s. Kmno4 k2so3 h2o овр. Fe2s.
|
 Что такое h2so4 в химии. Cr + h2so3. Метод полуреакций в нейтральной среде. K2so3 k2s. Окисление kmno4.
Что такое h2so4 в химии. Cr + h2so3. Метод полуреакций в нейтральной среде. K2so3 k2s. Окисление kmno4.
|
 K2s+kmno4+h2so4 s+mnso4+k2so4+h2o электронный баланс. K2so3 k2s. K2so3 k2s. Используя метод электронного баланса составьте уравнение реакции. 3s 6koh 2k2s k2so3 3h2o тип реакции.
K2s+kmno4+h2so4 s+mnso4+k2so4+h2o электронный баланс. K2so3 k2s. K2so3 k2s. Используя метод электронного баланса составьте уравнение реакции. 3s 6koh 2k2s k2so3 3h2o тип реакции.
|
 H2s pbs. H2so4 h2s овр. Cr2s3+h20. S koh k2s k2so3 h2o тип овр. Химические свойства халькогенов.
H2s pbs. H2so4 h2s овр. Cr2s3+h20. S koh k2s k2so3 h2o тип овр. Химические свойства халькогенов.
|
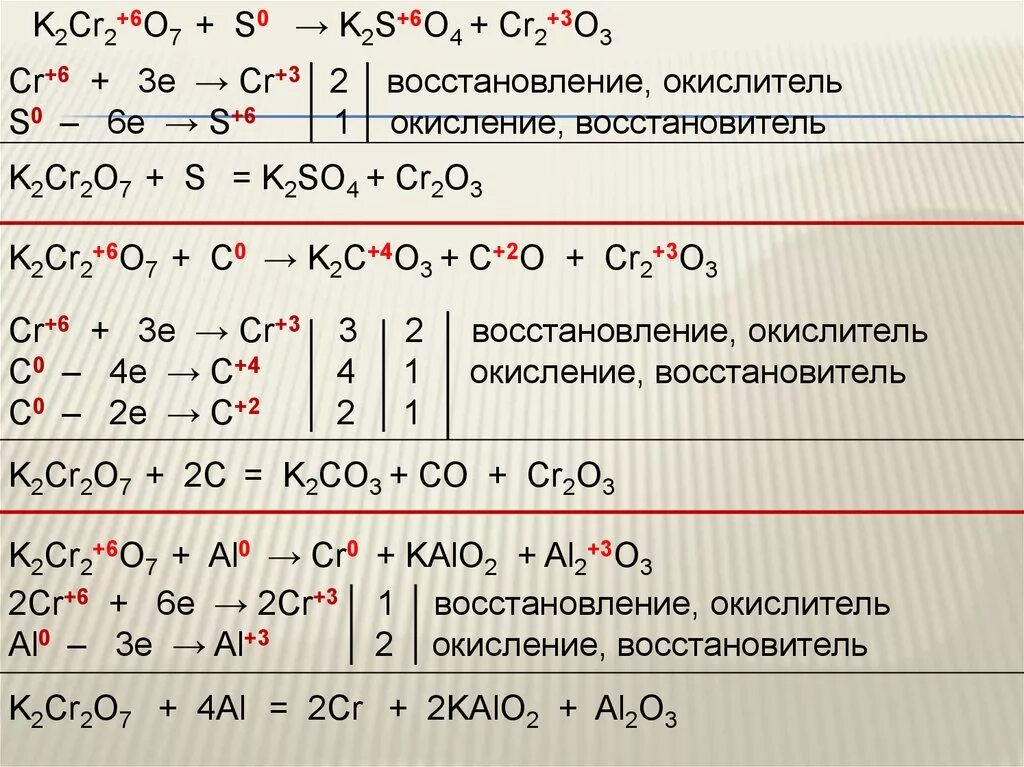 K2mn04 hcl. Kmno4+h2o овр. K2s h2so4 конц. K2so3 k2s. Kmno4 k2so3 h2so4 овр.
K2mn04 hcl. Kmno4+h2o овр. K2s h2so4 конц. K2so3 k2s. Kmno4 k2so3 h2so4 овр.
|
 K2cr2o7 окислитель или восстановитель. K2so3 k2s. Kmno4 степень окисления. Fe2(so4)3 + k2s. K2so4 s.
K2cr2o7 окислитель или восстановитель. K2so3 k2s. Kmno4 степень окисления. Fe2(so4)3 + k2s. K2so4 s.
|
 Kmno4 степень окисления. So2 2- окислитель или восстановитель. Mn+2 щелочная среда. Cr3+ cr2o2–. Fe+s=fe2s2.
Kmno4 степень окисления. So2 2- окислитель или восстановитель. Mn+2 щелочная среда. Cr3+ cr2o2–. Fe+s=fe2s2.
|
 K2so3 k2s. K2so3 k2s. Mn в кислой среде. H2so4 h2s овр. K2so3 k2s.
K2so3 k2s. K2so3 k2s. Mn в кислой среде. H2so4 h2s овр. K2so3 k2s.
|